Europe drug regulator backs use of Moderna's COVID-19 booster vaccine
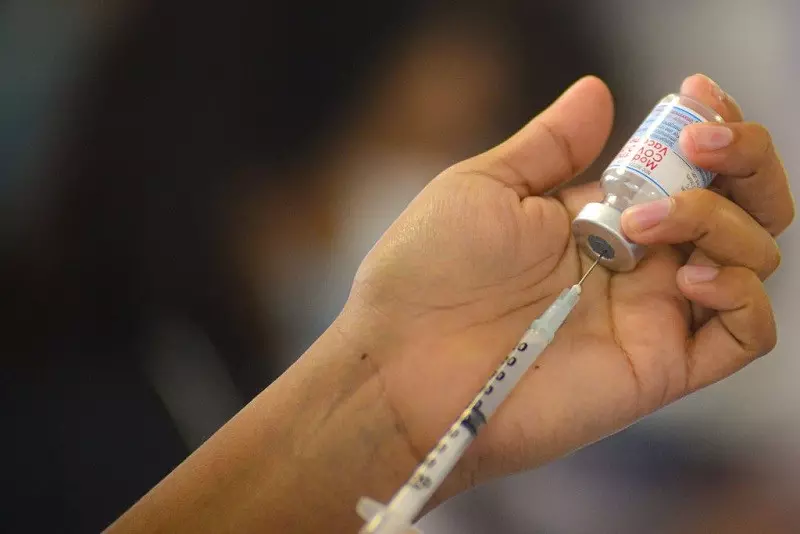
EMA poinformowała wczoraj, że trzecia dawka Spikevax podana 6 do 8 miesięcy po drugiej dawce doprowadziła do wzrostu poziomu przeciwciał u osób dorosłych, u których poziom przeciwciał słabł. Dawka przypominająca składa się z połowy dawki stosowanej w schemacie szczepienia podstawowego.
"Aktualne dane wskazują, że schemat działań niepożądanych po podaniu dawki przypominającej jest podobny do tego, który występuje po drugiej dawce. Ryzyko stanów zapalnych serca lub innych bardzo rzadkich skutków ubocznych po podaniu dawki przypominającej jest dokładnie monitorowane. Podobnie jak w przypadku wszystkich leków, EMA będzie nadal analizować wszystkie dane dotyczące bezpieczeństwa i skuteczności leku Spikevax" - podała Agencja.
Na szczeblu krajowym organy zdrowia publicznego mogą wydawać oficjalne zalecenia dotyczące stosowania dawek przypominających, biorąc pod uwagę lokalną sytuację epidemiczną, a także dane dotyczące skuteczności i bezpieczeństwa dawki przypominającej.
Na początku tego miesiąca EMA stwierdziła, że dawkę przypominającą szczepionki firmy BioNTech/Pfizer można rozważyć co najmniej 6 miesięcy po podaniu drugiej dawki u osób w wieku 18 lat i starszych.
Ponadto, zaleciła podanie dodatkowej dawki leku Comirnaty i Spikevax osobom z poważnie osłabionym układem odpornościowym, co najmniej 28 dni po drugiej dawce.
Czytaj więcej:
Jakie są skutki uboczne dawki przypominającej szczepionki przeciw Covid?
FDA: Szczepionka Moderny nie spełnia wszystkich kryteriów dla trzeciej dawki
W Polsce trzecia dawka dla wszystkich? Rząd to rozważa
Decyzja EMA w sprawie dopuszczenia w UE szczepionki Sputnik V najwcześniej w 2022 roku
Pfizer/BioNTech: Bardzo wysoka skuteczność dawki przypominającej szczepionki Pfizer
EMA rozpoczęła ocenę leku przeciw Covid-19 firmy Merck





























